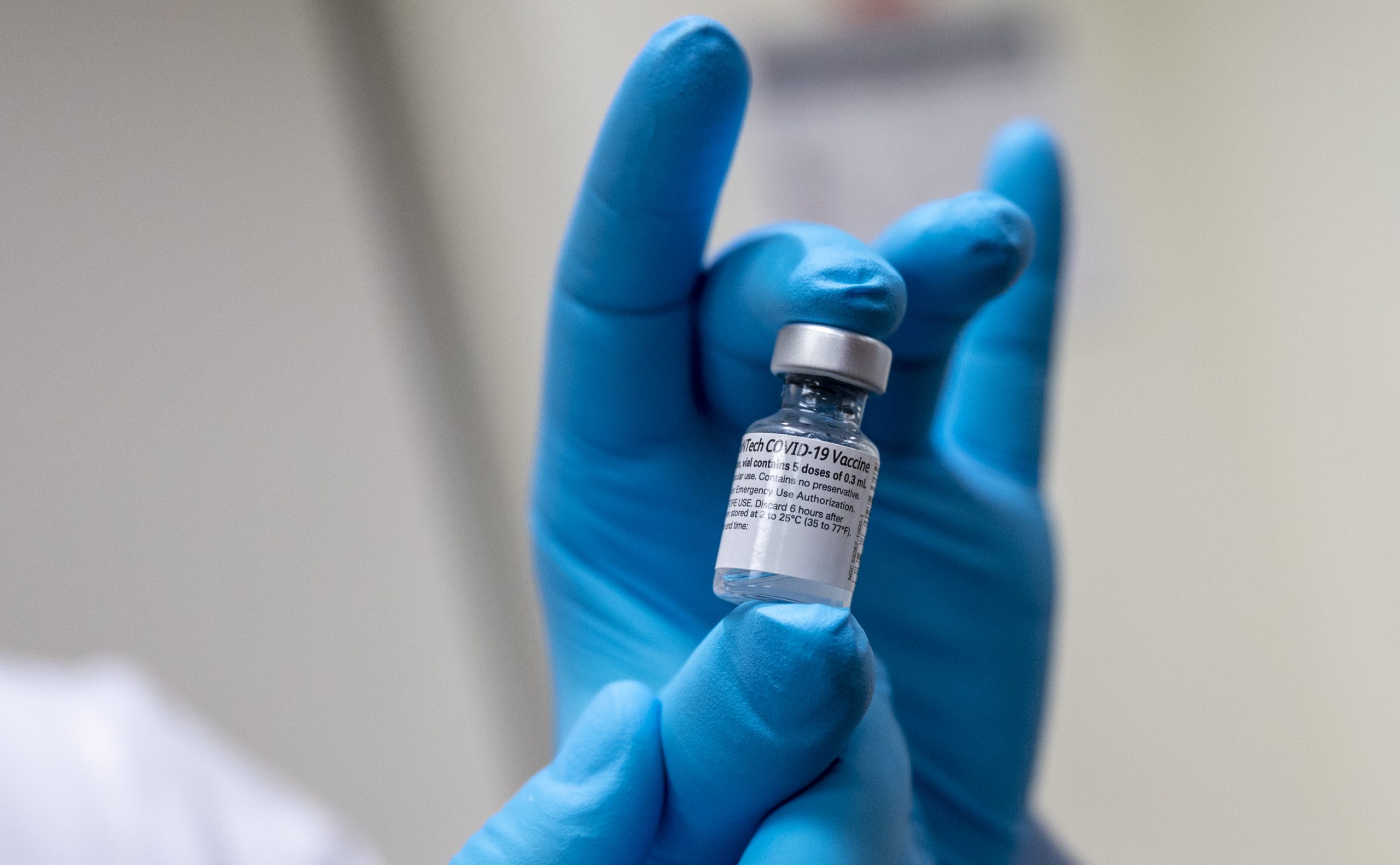
A Anvisa aprovou hoje (23.02) o primeiro registro definitivo de vacina no Brasil, a vacina da Pfizer, produzida em parceria com a Biontech.
Antes dessa aprovação, a Anvisa já tinha liberado a vacina Coronavac e a vacina de Oxford, apenas para uso emergencial. A vacina de Oxford também está em análise para aprovação de seu uso definitivo.
Após um período de análise de 17 dias, iniciado no dia 5 de fevereiro, o diretor da Anvisa, Antônio Barra Torres, informou por meio de nota, a aprovação do imunizante.
O que significa a obtenção do registro definitivo pela vacina da Pfizer?
Ao obter o registro definitivo, a partir de agora, está autorizado pela Anvisa que:
- a vacina da Pfizer poderá ser aplicada em todas as pessoas acima de 16 anos, e não apenas nos grupos prioritários, como é o caso da vacina de Oxford e da Coronavac, que apenas possuem o seu uso emergencial aprovado.
- este registro permite que a vacina seja importada pelo Brasil, uma vez que não existe a fabricação do imunizante no país, nem o contrato de negociação com a empresa prevê a transferência de tecnologia para que a vacina da Pfizer possa ser produzida no Brasil. As vacinas de Oxford e a Coronavac serão produzidas no Brasil, graças a acordos de transferência de tecnologia celebrados entre seus fabricantes e a Fiocruz e o Instituto Butantan.
Por que ainda não começou a imunização com a vacina da Pfizer?
Apesar da aprovação, a vacina da Pfizer ainda não está disponível no país, para imunização dos brasileiros, uma vez que ela ainda não foi adquirida pelo Ministério da Saúde, que é o órgão responsável pela compra de imunizantes no país.
Segundo o Ministro da Saúde, general Eduardo Pazuello, o motivo da compra da vacina da Pfizer ainda não ter sido realizada é a série de imposições feitas pela empresa. Em especial, a exigência de que conste no contrato uma cláusula de duração eterna e completa que exime a empresa fabricante de qualquer responsabilidade por efeitos colaterais advindos da aplicação da vacina.
Em justificativa, a Pfizer afirma que tais exigências estão em conformidade com os outros acordos celebrados em outras partes do mundo.
Para solucionar esse impasse, o Congresso está analisando a possibilidade de incluir na Medida Provisória que trata sobre a compra de vacinas um trecho onde o país assuma os riscos. Essa medida permite que o governo federal compre vacinas, mesmo antes da Anvisa liberar o registro definitivo ou temporário no Brasil.
Reunião entre Rodrigo Pacheco e representantes da vacina da Pfizer
Na última segunda-feira (22.02), o Presidente do Senado, Rodrigo Pacheco, participou de reunião com representantes da vacina da Pfizer e também da vacina fabricada pela Johnson & Johnson, para tentar viabilizar a aquisição destes imunizantes.
Após a reunião ele disse que iria conversar com o Ministro da Saúde para tentar viabilizar uma saída legislativa adequada para solucionar o impasse entre o governo e os fabricantes das vacinas. Desta forma, o Congresso poderia apresentar a segurança legal que o governo precisa para que possa incorporar as vacinas ao plano de imunização nacional contra a Covid-19.
Nota de aprovação da Vacina da Pfizer (Íntegra)
“Como Diretor-Presidente da Agência Nacional de Vigilância Sanitária, informo com grande satisfação que, após um período de análise de dezessete dias, a Gerência Geral de Medicamentos, da Segunda Diretoria, concedeu o primeiro registro de vacina contra a Covid 19, para uso amplo, nas Américas.
O imunizante do Laboratório Pfizer/Biontech teve sua segurança, qualidade e eficácia, aferidas e atestadas pela equipe técnica de servidores da Anvisa que prossegue no seu trabalho de proteger a saúde do cidadão brasileiro.
Esperamos que outras vacinas estejam em breve, sendo avaliadas e aprovadas. Esse é o nosso compromisso.”
Diretor-presidente Antonio Barra Torres